
Kontaktas:Klaida Džou (Ponas.)
Tel: plius 86-551-65523315
Mobilusis / WhatsApp: plius 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
El. paštas:sales@homesunshinepharma.com
Papildyti:1002, Huanmao Pastatas, Nr.105, Mengcheng Kelias, Hefėjus Miestas, 230061, Kinija
„AstraZeneca“ ir „Merck“&stiprintuvas; Co neseniai paskelbė „OlympiA“ (NCT02032823) 3 fazės tyrimo (NCT02032823), skirto adjuvantiniam tikslinio priešvėžinio vaisto Lynparza gydymui, rezultatus (olaparibas) gydant BRCA mutacijos didelės rizikos HER2 neigiamą ankstyvą krūties vėžiu sergančius pacientus. Duomenys rodo, kad lyginant su placebu, pagal Lynparza gydymą statistiškai reikšmingai ir kliniškai reikšmingai pagerėjo neinvazinės ligos išgyvenamumas (iDFS).
Verta paminėti, kad Lynparza yra pirmasis BRCA mutacijai skirtas vaistas, kuris kliniškai naudingas gydant adjuvantu. Apskaičiuota, kad 2020 metais krūties vėžys bus diagnozuotas 2,3 milijonui moterų visame pasaulyje, o BRCA mutacijos nustatomos maždaug 5% pacientų, sergančių krūties vėžiu. Apie 55-65% moterų, turinčių BRCA1 mutacijas, ir apie 45% moterų, turinčių BRCA2 mutacijas, krūties vėžys išsivystys iki 70 metų.
Dave'as Fredricksonas, „AstraZeneca“ onkologijos verslo skyriaus vykdomasis viceprezidentas, sakė: „Tai yra pirmas kartas, kai bet koks vaistas, nukreiptas į BRCA mutacijas, gali pakeisti ankstyvo krūties vėžio eigą ir suteikti vilties išgydyti. Pateikdami sprendimą, kuris gali žymiai sumažinti, mes tikimės, kad „Lynparza“ nustatys naują šių didelės rizikos pacientų krūties vėžio pasikartojimo rizikos gydymo etaloną ir parodys nuolatinę klinikinę naudą. Bendradarbiaujame su reguliavimo institucijomis, kad kuo greičiau pristatytume Lynparza šiems pacientams."
OlympiA yra dvigubai aklas, lygiagrečios grupės, placebu kontroliuojamas, daugiacentris 3 fazės tyrimas, skirtas įvertinti Lynparza tablečių ir placebo veiksmingumą ir saugumą adjuvantiškai gydant gBRCAm didelės rizikos HER2 neigiamą ankstyvą krūties vėžį. Šiems pacientams taikomas visiškas vietinis gydymas ir įprasta neoadjuvantinė ar pagalbinė chemoterapija. Pagrindinis tyrimo rezultatas yra iDFS, kuris apibrėžiamas kaip laikas nuo atsitiktinės atrankos iki pirmojo gydymo nesėkmės (vietinis ar tolimas pasikartojimas arba naujas vėžys arba mirtis dėl bet kokios priežasties).
Visoje tyrimo populiacijoje, lyginant su placebu, Lynparza 42% sumažino invazinio krūties vėžio pasikartojimo, antrojo vėžio ar mirties riziką (HR=0,58; 99,5% PI: 0,41-0,82; p< 0,0001).="" praėjus="" 3="" metams,="" 85,9%="" pacientų="" lynparza="" gydymo="" grupėje="" vis="" dar="" buvo="" gyvi="" ir="" be="" invazinio="" krūties="" vėžio="" bei="" antrojo="" vėžio,="" palyginti="" su="" 77,1%="" placebo="">
Be to, Lynparza statistiškai reikšmingai ir kliniškai reikšmingai pagerino pagrindinį antrinį išgyvenamumo be ligos (be ligos) (DDFS) antrinį tikslą, palyginti su placebu. Lynparza sumažino nuotolinės ligos pasikartojimo ar mirties riziką 43% (HR=0,57; 99,5% PI: 0,39-0,83, p< 0,0001).="" išankstinio="" duomenų="" nutraukimo="" metu="" tarp="" lynparza="" gydytų="" pacientų="" buvo="" mažiau="" mirčių,="" tačiau="" bendro="" išgyvenamumo="" (os)="" skirtumas="" nepasiekė="" statistinio="" reikšmingumo.="" tyrimo="" metu="" os="" bus="" toliau="" vertinamas="" kaip="" antrinis="" rezultatas.="" šio="" tyrimo="" metu="" lynparza="" saugumas="" ir="" toleravimas="" atitinka="" tuos,="" kurie="" buvo="" pastebėti="" ankstesniuose="" klinikiniuose="">
2021 m. Vasario mėn. Nepriklausomas duomenų stebėjimo komitetas (IDMC) rekomendavo „OlympiA“ bandymams pereiti prie išankstinės išankstinės analizės ir ataskaitų teikimo. Remdamasis suplanuota tarpine analize, IDMC padarė išvadą, kad tyrimas peržengė pagrindinį iDFS galutinio taško kraštą ir parodė tvarų, kliniškai reikšmingą Lynparza terapinį pranašumą, palyginti su placebu.
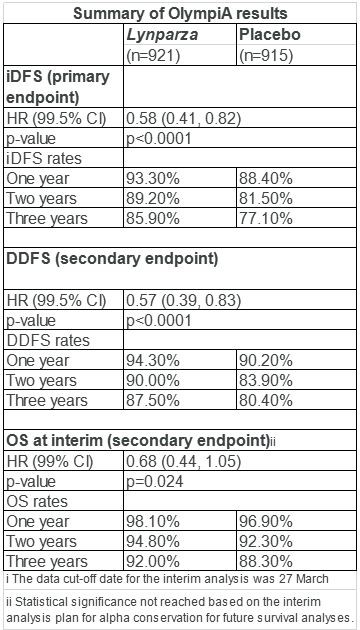
„OlympiA“ testo rezultatai
„Lynparza“ yra pirmasis tokio pobūdžio geriamasis poli-ADP ribozės polimerazės (PARP) inhibitorius, kuris gali pasinaudoti naviko DNR pažeidimų atstatymo (DDR) kelio defektais, norėdamas pirmiausia sunaikinti vėžines ląsteles. Šis veikimo būdas suteikia Lynparza gydymą, kurio DNR pažeidimo atstatymo defektai gali būti įvairaus tipo navikai (pvz., BRCA1 ir (arba) BRCA2 mutacijos).
2017 m. Liepos mėn. „AstraZeneca“ ir „Merck“ pasiekė pasaulinį strateginį bendradarbiavimą onkologijos srityje, kad kartu sukurtų ir komercializuotų „Lynparza“ ir kitą MEK inhibitorių.selumetinibasgydyti įvairiausius navikus, įskaitant krūties, prostatos ir kasos vėžį.
Lynparza (olaparibas) yra pirmasis pasaulyje' PARP inhibitorius, kurį JAV FDA pirmą kartą patvirtino 2014 m. gruodžio mėn. Iki šiol „Lynparza“ buvo patvirtinta 7 gydymo indikacijoms: su BRCAm pažengusiu kiaušidžių vėžiu; (2) kombinuotas pirmosios eilės bevacizumabo palaikomasis gydymas suaugusiesiems, sergantiems pažengusiu širdies nepakankamumu, progresavusiu kiaušidžių vėžiu; (3) palaikomoji terapija Suaugę pacientai, sergantys pasikartojančiu kiaušidžių vėžiu; (4) Suaugę pacientai, sergantys pažengusiu gBRCAm kiaušidžių vėžiu; (5) gBRCAm, HER2 neigiamų (HER2) suaugusių pacientų, sergančių metastazavusiu krūties vėžiu, gydymas; (6) Pirminis palaikomasis gydymas suaugusiesiems, sergantiems gBRCAm metastazavusiu kasos vėžiu; (7) Pacientų, sergančių metastazavusiu kastracijai atspariu prostatos vėžiu (mCRPC), turinčių specifinių genų mutacijų, gydymas.
Kinijoje „Lynparza“ (olaparibas) buvo patvirtintas 2018 m. rugpjūčio mėn. palaikomajam platinai jautraus pasikartojančio kiaušidžių vėžio gydymui. „Lynparza“ yra pirmasis tikslinis vaistas, patvirtintas kiaušidžių vėžiui gydyti Kinijos rinkoje, žymintis Kinijos' kiaušidžių vėžio gydymą, įžengiantį į PARP inhibitorių erą. 2019 m. Gruodžio pradžioje Lynparza vėl buvo patvirtintas pirmojo pasirinkimo palaikomajam gydymui pacientams, sergantiems BRCA mutavusiu išplitusiu kiaušidžių vėžiu. Kinija gauna didelę paramą farmacijos naujovėms ir greitina kliniškai reikalingus naujus vaistus. „Lynparza“ tapo pirmuoju PARP inhibitoriumi, patvirtintu pirmosios eilės kiaušidžių vėžio palaikomajam gydymui Kinijoje. 2019 m. Lapkričio 28 d. „Lynparza“ buvo įtraukta į Nacionalinę medicinos draudimo katalogą.